What is Vapour Pressure in Hindi | वेपर प्रेशर इन हिंदी | क्या है वेपर प्रेशर?
वेपर प्रेशर (Vapour Pressure)
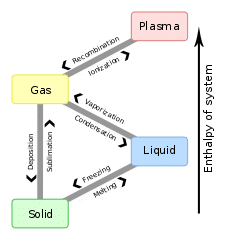
जब कोई तरल (Liquid)पदार्थ या फिर सॉलिड(Solid) वस्तु अपने वेपर रूप में सतह की तरफ बढ़ती है उस स्थिति में जो प्रेशर बनता है उसे वेपर प्रेशर कहते हैं। बढ़ते तापमान के साथ वेपर प्रेशर बढ़ जाता है। किसी भी वस्तु के वेपर में बदलने पर सतह पर प्रेशर बढ़ जाता है। समय की एक कड़ी पर सतह का प्रेशर यानि दबाव आसपास के दबाव के बराबर होने लगता है। इस स्थिति में लिक्विड बॉईल होने लगेगा। ये तापमान उस तरल का बोइलिंग पॉइंट (Boiling Point) कहलाएगा।
वेपर प्रेशर से जुड़े रोचक तथ्य (Characteristics of Vapour Pressure)
बढ़ते हुए समय के साथ किसी भी तरल को उबालने पर अणुओं की मात्रा में इजाफा हो जाता है जिसके फलस्वरूप कंडेंसशन प्रक्रिया भी बढ़ जाती है। वाष्पीकरण और कंडेंसशन की प्रक्रिया का रेट समान होने पर स्थिति सामानांतर यानि एक़्विलिब्रियम (Equilibrium) कहलात्ती है।
वेपर प्रेशर किन बातों पर निर्भर करता है ? (Factors affecting Vapour Pressure)
१. तरल का व्यवहार (Nature of Solvent)
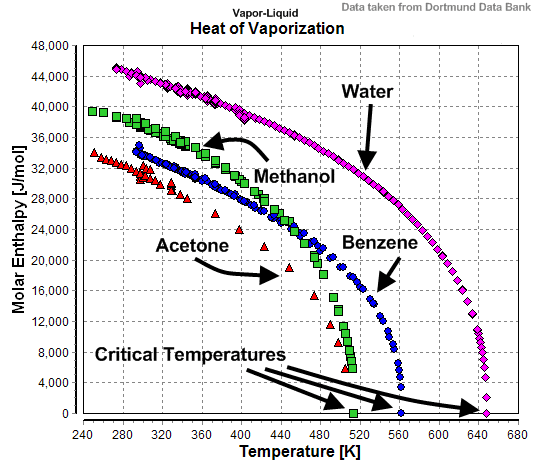
तरल के मॉलीक्यूल्स आपस में एक दूसरे से बहुत दूर होते हैं। इस वजह से ये अधिक भाप बना पाते हैं। कई बार मिश्रण और तरल पानी से भी अधिक भाप बना पाते हैं। जैसे कि बेंजीन और एसीटोन का मिश्रण। एक निर्धारित तापमान पर एसीटोन और बेंजीन के मिश्रण का वेपर प्रेशर पानी से अधिक होता है।
२. तापमान (Temprature)
बढ़ते हुए तापमान की वजह से वेपर प्रेशर भी बढ़ जाता है।
विशेषता तरल पदार्थों का वाष्प दबाव (Vapour Pressure of Characteristic Liquids)
| Fluid Name | Vapor Pressure (kPa) |
| Acetaldehyde | 120 |
| Acetic acid | 2.1 |
| Acetic acid anhydride | 0.68 |
| Acetone | 30 |
| Allyl alcohol | 2.3 |
| Allyl chloride | 40 |
| Aluminum nitrate, 10% solution in water | 2.4 |
| Aluminum sulphate, 10% solution in water | 2.4 |
| Amyl acetate | 0.47 |
| Aniline | 0.09 |
| Beer | 2.4 |
| Benzene | 14 |
| Benzyl alcohol | 0.013 |
| Bromine | 28 |
| Butyl acetate | 1.5 |
| Butyl alcohol, 1-butanol | 0.93 |
| Butyric acid n | 48 |
| Calcium chloride, 25% solution in water | 2.4 |
| Calcium chloride, 5% solution in water | 2.4 |
| Carbon disulphide | 48 |
| Carbon tetrachloride | 15.3 |
| Chloroform | 26 |
| Cyclohexanol | 0.9 |
| Cyclohexanone | 0.67 |
| Ethyl acetate | 14 |
| Ethyl alcohol | 12.4 |
| Ethyl glycol | 0.7 |
| Ethylene glycol | 0.007 |
| Formic acid | 5.7 |
| Furfurol, 2-Furaldehyde | 0.3 |
| Heptane | 6 |
| Hexane | 17.6 |
| Isopropyl alcohol (rubbing alcohol) | 4.4 |
| Kerosene | 0.7 |
| Methyl acetate | 28.8 |
| Methyl alcohol, methanol | 16.9 |
| Methylene chloride, dichloromethane | 58 |
| Milk | 2.4 |
| Nitrobenzene | 0.03 |
| Nonane | 0.6 |
| Octane | 1.9 |
| Pentane | 58 |
| Phenol | 0.05 |
| Propanol | 2.8 |
| Propionic acid | 0.47 |
| Seawater | 2.4 |
| Sodium chloride, 25% solution in water | 2.4 |
| Sodium hydroxide, 20% solution in water | 2.4 |
| Sodium hydroxide, 30% solution in water | 2.4 |
| Styrene | 0.85 |
| Tetrachloroethane | 0.7 |
| Tetrachloroethylene | 2.5 |
| Toluene | 3.8 |
| Trichloroethylene | 9.2 |
| Water | 2.4 |
Raoults’s Law
पी 1 α एक्स 1
P1 = P1o X1, ……………………………। (1)
जहां P1o शुद्ध अवस्था में घटक 1 का वाष्प दाब है।
इसी तरह घटक 2 के लिए:
पी 2 = पी 2 एक्स 2, …………………………… .. (2)
डाल्टन के आंशिक दबावों के नियम से हम जानते हैं कि,
Ptotal = P1 + P2
पी 1 और पी 2 के मूल्यों का उपयोग करते हुए क्रमशः समीकरण (1) और (2) हमारे पास है:
Ptotal = P1ox1 + P2ox2
=> Ptotal = P1o (1-x2) + P2ox2
=> Ptotal = P1o + (P2o-P1o) x2
हम उपरोक्त समीकरण से निम्नलिखित निष्कर्ष निकाल सकते हैं:
- उपरोक्त समीकरण Ptotal और x2 के बीच एक सीधी रेखा है जिसका ढलान (P2o-P1o) द्वारा दिया गया है और y- अवरोधन P1o के बराबर है।
- एक समाधान के ऊपर कुल वाष्प दबाव घटक 2 के मोल अंश के साथ रैखिक रूप से भिन्न होता है।
- एक घोल के ऊपर का कुल वाष्प दाब उनकी शुद्ध अवस्था में घटक 1 और 2 के वाष्प दाब पर निर्भर करता है और घोल में घटक 2 का मोल अंश।
बोइलिंग पॉइंट क्या है? (What is Boiling Point?)
तरल पदार्थों का तापमान बढ़ाने पर वेपर प्रेशर में वृद्धि हो जाती है। एक स्टेज पर आने के बाद तरल का वेपर प्रेशर और वातावरण का प्रेशर एक सामान हो जाता है। इस तापमान को बोइलिंग पॉइंट कहते हैं।
स्टैण्डर्ड बोइलिंग पॉइंट ऑफ़ लिक्विड (Standard Boiling point of liquid)
प्रेशर ऑफ़ 1 atm = 102325 पास्कल (Pa)
हीट ऑफ़ वैपराइज़शन क्या है? (What is Heat of Vaporization?)
तरल को गरम करने पर उसकी एनर्जी में खास वृद्धि हो जाती है। 1 मोल लिक्विड को गरम करने पर वो वाष्प में परिवर्तित हो जाता है। ऐसा होने में जितनी गर्मी या ऊर्जा का उपयोग होता है वही हीट ऑफ़ वैपोराइजैशन कहलाता है।
वाष्प का दबाव तरल पदार्थों के सबसे महत्वपूर्ण गुणों में से एक है। इसका उपयोग समाधान की गलतफहमी, स्थिरता और विभिन्न अन्य गुणों को निर्धारित करने के लिए किया जाता है जो रासायनिक प्रतिक्रिया परिणामों को महत्वपूर्ण रूप से बदल सकते हैं।
इसलिए, यहां हमने वाष्प दबाव और संबंधित विवरणों पर चर्चा की है।
समाधान और संबंधित अवधारणाओं के पीछे विज्ञान के बारे में अधिक जानने के लिए hindi.todaysera.com/category/science/ से जुड़े रहें.