प्रोटॉन के संबंध में इलेक्ट्रॉन और उनकी प्रासंगिकता (Electrons and its relevance with respect to Protons) | Electrons Kya Hote Hain
हमारे आसपास के अलग – अलग तरह की प्रक्रियाएं जैसे कि प्रकाश, मेटल का चमकना और इनकी कंडक्शन की प्रॉपर्टी सभी में इलेक्ट्रॉन्स महत्त्वपूर्ण भाग निभाते हैं। आने वाले दिनों में इनसे जुड़े और भी कई रहस्य रिसर्च में पता लगाए जाएंगें। आइए जानते हैं इनके गुण और रोचक तथ्य।
इलेक्ट्रॉन क्या हैं? (What are electrons?)
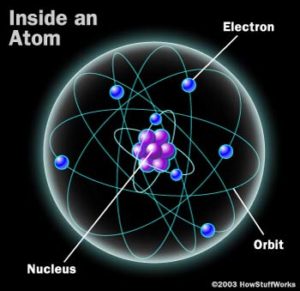
- इलेक्ट्रॉन एक उप-परमाणु कण होते हैं जो एक परमाणु के नाभिक की परिक्रमा करते हैं। वे आम तौर पर नकारात्मक चार्ज होते हैं और परमाणु के नाभिक से बहुत छोटे होते हैं। यदि आप सूरज की तुलना में पृथ्वी के आकार की तुलना में एक उचित आकार चाहते हैं, तो यह एक बहुत करीबी दृश्य होगा।
- इलेक्ट्रॉनों को कक्षाओं या ऊर्जा स्तरों में गिरने के लिए जाना जाता है। ये कक्षाएँ किसी ग्रह या आकाशीय पिंड की कक्षा की तरह दिखाई नहीं देती हैं। कारण यह है कि परमाणु कुख्यात रूप से छोटे होते हैं और सबसे अच्छे सूक्ष्मदर्शी केवल इतने बड़े पैमाने पर परमाणुओं को देख सकते हैं।
- यहां तक कि अगर हम इलेक्ट्रॉनों को देख सकते हैं, तो वे मानव आंखों के लिए बहुत तेजी से आगे बढ़ेंगे। वास्तव में, वैज्ञानिक अभी भी इलेक्ट्रॉनों की सही स्थिति की गणना नहीं कर सकते हैं।
- वे केवल अपने स्थानों का अनुमान लगा सकते हैं। यही कारण है कि परमाणुओं के आधुनिक मॉडल में एक संकेंद्रित कक्षाओं में इलेक्ट्रॉनों की परिभाषित प्रणाली के बजाय एक परमाणु के नाभिक के आसपास एक इलेक्ट्रॉन बादल होता है।
इलेक्ट्रॉनों का महत्व, खोज और महत्वपूर्ण तथ्य (Discovery of electrons, importance and Facts)
इलेक्ट्रॉन एक नकारात्मक रूप से चार्ज होने वाला उप-परमाणु कण है जो परमाणुओं का एक महत्वपूर्ण घटक है जो सामान्य पदार्थ बनाते हैं। इलेक्ट्रॉन मौलिक है, इसमें यह नहीं माना जाता है कि यह छोटे घटकों से बना है। इलेक्ट्रॉन पर आवेश का आकार प्रकृति में पाए जाने वाले आवेश की मूलभूत इकाई माना जाता है।
सभी विद्युत आवेशों को इस आवेश का अभिन्न गुणक माना जाता था। हाल ही में, हालांकि, यह बताने के लिए पर्याप्त सबूत पाए गए हैं कि मेसंस और बेरियन के रूप में वर्गीकृत किए गए कण क्वार्क नामक वस्तुओं से बने होते हैं, जिनमें इलेक्ट्रॉन पर चार्ज 2/3 या 1/3 होता है।
उदाहरण के लिए, न्यूट्रॉन और प्रोटॉन, जो परमाणुओं के नाभिक का निर्माण करते हैं, बेरियन हैं। हालांकि, वैज्ञानिक कभी भी एक पृथक क्वार्क का निरीक्षण नहीं कर पाए हैं, इसलिए सभी व्यावहारिक उद्देश्यों के लिए इलेक्ट्रॉन पर प्रभार अभी भी प्रकृति में पाए जाने वाले चार्ज की मूलभूत इकाई माना जा सकता है।
इस चार्ज की परिमाण, जिसे आमतौर पर ई द्वारा नामित किया गया है, को बहुत सटीक रूप से मापा गया है और यह 1.602177 × 10-19 कूपोम है। इलेक्ट्रॉन का द्रव्यमान परमाणु मानकों से भी छोटा होता है और इसका मूल्य 9.109389 × 10-31 किग्रा (0.5110 M V / c2 e) होता है, केवल प्रोटॉन का द्रव्यमान 1/1836 होता है।
प्रकृति में पाए जाने वाले सभी परमाणुओं में एक सकारात्मक रूप से चार्ज किया गया नाभिक होता है, जिसके बारे में नकारात्मक चार्ज किए गए इलेक्ट्रॉन चलते हैं। परमाणु विद्युत रूप से तटस्थ होता है और इस प्रकार नाभिक पर धनात्मक विद्युत आवेश सभी इलेक्ट्रॉनों के कारण ऋणात्मक आवेश के समान परिमाण होता है।
इलेक्ट्रॉनों को परमाणु में सकारात्मक रूप से चार्ज किए गए नाभिक द्वारा उन पर लगाए गए आकर्षक बल द्वारा आयोजित किया जाता है। वे कक्षा में नाभिक के बारे में बहुत तेज़ी से आगे बढ़ते हैं, जिसमें बहुत निश्चित ऊर्जा होती है, जिससे चारों ओर इलेक्ट्रॉन बादल बन जाते हैं। एक विशिष्ट परमाणु में कुछ इलेक्ट्रॉन नाभिक के काफी करीब हो सकते हैं, जबकि अन्य दूरी पर हो सकते हैं जो नाभिक के व्यास से कई हजार गुना बड़े होते हैं।
इस प्रकार, इलेक्ट्रॉन बादल चित्रा 1. हंस और कैसिडी द्वारा चित्रण निर्धारित करता है। गेल ग्रुप के सौजन्य से परमाणु का आकार। यह सबसे बाहरी इलेक्ट्रॉन है जो विभिन्न तत्वों के रासायनिक व्यवहार को निर्धारित करता है। परमाणुओं के चारों ओर इलेक्ट्रॉन बादलों का आकार और आकार केवल भौतिकी के एक क्षेत्र का उपयोग करके समझाया जा सकता है जिसे क्वांटम यांत्रिकी कहा जाता है।
धातुओं में इलेक्ट्रॉन गतिविधि (Activity of electrons in metals – Electricity Conduction)
धातुओं में, कुछ इलेक्ट्रॉन कसकर परमाणुओं से बंधे नहीं होते हैं और एक विद्युत क्षेत्र के प्रभाव में धातु के माध्यम से स्थानांतरित करने के लिए स्वतंत्र होते हैं। यह इस स्थिति है कि इस तथ्य के लिए जिम्मेदार है कि अधिकांश धातुएं बिजली और गर्मी के अच्छे संवाहक हैं।
क्वांटम सिद्धांत भी इलेक्ट्रॉनों के बजाय कई अन्य अजीब गुणों की व्याख्या करता है। इलेक्ट्रॉन व्यवहार करते हैं जैसे कि वे कताई कर रहे थे, और इस स्पिन से जुड़े कोणीय गति का मूल्य तय हो गया है; इस प्रकार यह आश्चर्यजनक नहीं है कि इलेक्ट्रॉन भी छोटे चुम्बकों की तरह व्यवहार करते हैं।
जिस तरह से कुछ सामग्रियों जैसे कि लोहे में इलेक्ट्रॉनों को व्यवस्थित किया जाता है, इन सामग्रियों को चुंबकीय बनाता है। पॉज़िट्रॉन के अस्तित्व, इलेक्ट्रॉन के एंटीपार्टिकल, की भविष्यवाणी 1930 में फ्रांसीसी भौतिक विज्ञानी पॉल डिराक ने की थी। इस एंटीप्रार्टिकल की भविष्यवाणी करने के लिए, उन्होंने क्वांटम यांत्रिकी के एक संस्करण का उपयोग किया जिसमें सापेक्षता के सिद्धांत के प्रभाव शामिल थे।
आइंस्टीन के मास-ऊर्जा समतुल्य व्याख्या -Einstein’s Mass-Energy Equivalence Explained
पॉज़िट्रॉन के आवेश में इलेक्ट्रॉन के आवेश के समान परिमाण होता है लेकिन धनात्मक होता है। डायराक की भविष्यवाणी को दो साल बाद सत्यापित किया गया था, जब पोसिट्रॉन को कार्ल एंडरसन द्वारा प्रायोगिक तौर पर कॉस्मिक किरणों पर अनुसंधान के लिए उपयोग किए जाने वाले क्लाउड कक्ष में देखा गया था।
पॉज़िट्रॉन सामान्य पदार्थ की उपस्थिति में बहुत लंबे समय तक मौजूद नहीं होता है क्योंकि यह जल्द ही एक साधारण इलेक्ट्रॉन और दो कणों के संपर्क में आता है, दो इलेक्ट्रॉन द्रव्यमान के बराबर ऊर्जा के बराबर एक गामा किरण का उत्पादन करता है, जिसके अनुसार आइंस्टीन का प्रसिद्ध समीकरण E = mc2।
इलेक्ट्रॉनों की प्रतिक्रियाएं (Reactions of Electrons)
केवल बाहरी आवरण या वैलेंस शेल में इलेक्ट्रॉन ही रासायनिक प्रतिक्रियाओं में भाग लेते हैं। … बाहर की घाटी के गोले में इलेक्ट्रॉनों का निर्धारण होता है कि एक परमाणु कैसे व्यवहार करता है, चाहे वह रासायनिक प्रतिक्रियाओं में भाग लेने के लिए इलेक्ट्रॉनों को ले या साझा कर रहा हो, दो प्रकार के रासायनिक बांड बनाता है:
आयनिक और सहसंयोजक
ऑक्सीकरण और न्यूनीकरण प्रक्रियाएँ (Oxidation & Reduction Reactions)
ऑक्सीकरण इलेक्ट्रॉनों की हानि या एक अणु में एक परमाणु, आयन या कुछ परमाणुओं के ऑक्सीकरण राज्य में वृद्धि है। (Oxidation)
कटौती इलेक्ट्रॉनों का लाभ है या एक अणु में एक आयन, या कुछ परमाणुओं के ऑक्सीकरण राज्य में कमी है।(Reduction)
ऑक्सीकरण में एक परमाणु के ऑक्सीकरण संख्या में वृद्धि शामिल है।
न्यूनीकरण तब होता है जब किसी परमाणु का ऑक्सीकरण संख्या घट जाता है।
इस मॉडल के अनुसार, हाइड्रोजन के साथ प्रतिक्रिया करने पर CO2 कम हो जाती है क्योंकि कार्बन का ऑक्सीकरण संख्या +4 से घटकर 2 हो जाता है। इस प्रतिक्रिया में हाइड्रोजन का ऑक्सीकरण होता है क्योंकि इसकी ऑक्सीकरण संख्या 0 से +1 तक बढ़ जाती है।
इलेक्ट्रॉन हस्तांतरण प्रतिक्रिया का उदाहरण(Example of Electron Transfer Reaction )
जब आयरन (स्टील ऊन) को CuSO4 के घोल में रखा जाता है तो प्रतिक्रिया नीचे दी गई तालिका में दिखाई जाती है।
स्टील ऊन में मुख्य रूप से Fe परमाणु होते हैं।
Cu2 + आयन एक CuSO4 घोल को अपने नीले रंग का देता है।
→ स्टील ऊन को धातु के क्यू के साथ लेपित किया जाता है जहां इसे CuSO4 के घोल में डुबोया जाता है।
समाधान रंग खो देता है क्योंकि Cu2 + को बेरंग Fe2 + आयनों द्वारा विस्थापित किया गया है।
Cu2+ + Fe → Cu + Fe2+
अगर आपको हमारी यह पोस्ट इलेक्ट्रान क्या है इन हिंदी | What is the Electron in Hindi? पसंद आई है तो इस पोस्ट को फेसबुक, Instagram और Pintrest पे share करें।
रासायनिक विज्ञानं से जुड़ी और अधिक जानकारी के लिए hindi.todaysera.com/category/science/ से जुड़े रहें।